2022年9月2日君实生物(688180)发布公告称公司于2022年8月31日召开业绩说明会,中信证券、长盛基金、至璞资产、上海留仁资产管理有限公司、建银国际资管、北京金百镕投资管理有限公司、广发基金、璟恒投资、Sumitomo Mitsui DS Asset Management、昊泽致远、银杏环球、涌金资管、LYZZ Capital、诚盛投资、大家资产、乐信资产、青岛鲁创投资管理有限公司、中邮证券、瞰渡资产、景领投资、先锋基金、上投摩根基金、鑫翰资本、绿地金融、通用技术、海创药业、尚诚资产、中泰证券资管、新华资产管理、福建省国资投资基金管理有限公司、凯石基金、众诚汽车保险股份有限公司、财通证券、易正郎投资、Point72、名禹资产、华泰柏瑞基金、景林资产、长乐汇资本、和谐汇一、前海开源、基石药业、鹏圆资产、胤胜资产、科兴制药、源乘投资、中债信用增进投资、锐智资本、上海宁泉资产、路博迈、宁银理财、上海证券、海南拾玉投资、昭时投资、东吴证券、西部证券自营、美国华平投资、笃诚投资、中泰证券、安远医药、上汽颀臻、英大国际信托、国盛证券、招银理财、浙商证券、惠正投资、深圳前海智申资产、ajsecurities、万家基金、野村证券资管部、海通证券、嘉实基金、磐泽资产、仁布投资、荣源大方投资有限公司、才华资本、百川投资、北京煜诚私募基金、永唐盛世资产、百泓投资、瓴仁投资、HHLR、禾其投资、峰境基金、鼎鉴投资、承泽资产、中金瑞丰、鹏万投资、兴亿投资、AIHC Capital Management、安信证券、双安资产、光大证券、卓财投资、韶夏资本、太朴生科基金、广东民营投资股份有限公司、华融证券、上海磐厚、盘京投资、前海联合基金、傲鹰投资、前海智申资产、艾博生物、红杉资本、创金合信、远信投资、中邮创业基金、峰之魁投资、禾盛投资、中银证券、上海国资公司、挪威中央银行、壹丰投资、海宸投资、河清资本、君茂资本、伯兄投资、中信期货有限公司、神农投资北京、理成资产、同犇投资、利幄基金、国泰人寿、混沌道然资产、中信建投、东方证券、Janchor Partners、宏鼎财富、复宏汉霖、申万菱信基金、Kaison Asset Management Group、华能贵诚信托、睿远基金、九泰基金、红点影视、Sino-Ocean Group、如今投资、安信资管、禾丰正则、雪石资产、彼得明奇、北京奥天奇投资、Taikang AMC、Opera Limited、紫阁投资、昆仑万维资本、东海自营、成泉资本、乘安资产、乾瞻资本、丰琰投资、博鸿投资、九方资本、天弘基金、国联安基金、上海世诚投资、方正证券、韶夏投资、汇华理财、东方自营、中信资管、固禾投资、远望角投资、广汇缘资产、申万宏源资管、汇添富基金、加拿大鲍尔公司、红筹投资、沣杨资产、中信里昂、中欧基金、Polymer Capital、国金证券、Teng Yue Partners、富国基金、碧云资本、招商证券香港、由榕资产、EarnestPartners、逸原达投资、涌容资产、立青投资、博裕资本、广发证券、国寿养老、华宝基金、高能资本、Ariose Capital 弘盛资本、中加基金管理有限公司、深梧资产、Auerbach Grayson、SPDBI、东海证券、天虫资本、中银资管、申万宏源证券、拾贝投资、ZH Securities Limited、光大保德信基金、永禧投资、庶达资产、China Alpha Fund Management (HK) Limited、CSFG International Asset Management、域秀资产、和达创投、纳锘实业、中金公司、国寿安保基金、Dongxing Securities、华安证券、Matthews Asia、红土创新基金、民森投资、华大、华夏基金、华宸未来、诺安基金、天安财险、平安证券、平安养老保险、3W Fund、乐赢基金、康曼德资本、广东塔牌创业投资管理有限公司、上海人寿、中资东方(北京)投资基金管理有限公司、AIHC Capital、长江证券(自营)、海通机构与国际业务部、元昊投资、奥博资本、高毅资产、瑞银资管、上海榜样投资管理有限公司、Aberdeen Standard Investments (Asia)、Platina Capital Management、进化论资产、TruMed Investments、清池资本(香港)、Horizon Asset International (HK)、景泰利丰、Causeway、第一北京投资、阳光资产、上海保银投资、Prudence Investment参与。
具体内容如下:
问:特瑞普利单抗国内的商业化预期?
答:2022年上半年,特瑞普利单抗在国内的销售已走出低谷,2022年一季度销售收入较2021年四季度环比提升约212%。虽然在4至5月受到了上海、吉林等地区疫情影响,2022年第二季度销售收入仍然环比一季度提升约70%。商业化团队也基本调整到位,人数超过1,100人。
公司认为,随着更多同类产品的获批上市,未来国内PD-1的商业化竞争将更多地比拼适应症覆盖和药物自身的疗效及安全性。从已披露的安全性和有效性数据来看,特瑞普利单抗具有显著优势,同时,除已获批的小适应症外,公司积极推进肺癌、肝癌、食管癌、乳腺癌等病患群体较大的适应症一线治疗以及围手术期/术后辅助治疗的临床试验,以为商业化推广提供更扎实的基础。 2022年5月,特瑞普利单抗联合紫杉醇和顺铂用于不可切除局部晚期/复发或远处转移性食管鳞癌患者的一线治疗获得NMP批准,这是国内获批的第五项适应症。2021年12月,特瑞普利单抗联合化疗用于一线治疗无EGFR或LK突变的晚期非小细胞肺癌患者的新适应症上市申请获得NMP受理,并有望于2022年获批。此外,一线小细胞肺癌、一线肝癌、肝癌术后辅助、非小细胞肺癌围手术期治疗的三期临床也有望于2022年进行数据读出,公司将在数据读出后尽快启动与药监部门的沟通,积极推动大适应症的获批上市。 未来,公司将根据市场竞争情况积极调整市场推广策略,继续投入医患教育,以增强市场对免疫疗法的认知,提升医生选择创新的免疫疗法的信心,建立特瑞普利单抗在医生与患者中的口碑。并积极扩大适应症、同步探索单药和联合免疫治疗,以扩大病患服务群体,争取更多市场份额。公司希望能够稳扎稳打,在踏实做好推广的同时继续将销售费用控制在合理水平,实现销售的可持续增长。随着更多大适应症进入获批阶段,多适应症围手术期临床研究的前瞻性布局优势渐显,公司团队有信心拿到应该取得的市场份额,实现销售收入的持续快速增长。
问:FDA对特瑞普利单抗的上市审评进展如何?
答:2022年7月,FD受理了公司重新提交的特瑞普利单抗联合吉西他滨/顺铂作为晚期复发或转移性鼻咽癌患者的一线治疗和单 药用于复发或转移性鼻咽癌含铂治疗后的二线及以上治疗的BL。FD已将PDUF的目标审评日期定为2022年12月23日。
基于目前的疫情管控政策,现场检查时间存在不确定性,公司将继续保持与FD和地方政府的积极沟通,争取达成可协调的方案。公司的合作伙伴Coherus也已开始对上市后的商业化工作进行筹备,如获批准,Coherus计划于2023年第一季度在美国推出特瑞普利单抗,特瑞普利单抗也将成为美国首个且唯一用于鼻咽癌治疗的肿瘤免疫药物。
问:VV116的临床和审批进展?
答:公司已完成一项VV116对比奈玛特韦片/利托那韦片(即PXLOVID)用于轻中度COVID-19患者早期治疗的有效性和安全性的多中心、单盲、随机、对照III期临床研究(NCT05341609)。研究结果显示,VV116用于轻中度COVID-19伴有进展为重度包括死亡的高风险患者早期治疗达到方案预设的主要终点和次要有效性终点。在主要终点方面,VV116组中位至持续临床恢复时间更短,达到统计学优效。在次要有效性终点方面,VV116组和PXLOVID组均未发生COVID-19疾病进展及死亡。同时研究结果也显示两组至持续临床症状消失时间,以及至首次SRS-CoV-2核酸转阴时间相似,相比于PXLOVID,VV116组有统计学优效趋势。安全性方面,VV116在人体试验临床显示出令人满意的安全性和耐受性,在头对头三期研究中整体不良事件发生率低于PXLOVID,安全性良好。
公司与旺山旺水还开展了一项针对中重度COVID-19的VV116对比标准治疗的有效性和安全性的国际多中心、随机、双盲III期临床研究,以及一项针对轻中度COVID-19的国际多中心、双盲、随机、安慰剂对照的III期临床研究(NCT05242042),上述两项临床试验均在进行中。 此外,2022年5月18日,VV116在中国奥密克戎感染者中首个临床研究结果发表于Emerging Microbes& Infection杂志。该临床试验为一项开放性、前瞻性队列研究,评估VV116对非重症奥密克戎感染者SRS-CoV-2核酸转阴时间的影响。研究数据提示1)在所有受试者中,VV116组核酸转阴时间为9.92天(VS.对照组11.13天);2)从开始用药到核酸转阴平均时间为3.52天;3)在首次核酸检测阳性5日内使用VV116的受试者中,其核酸从首次检测阳性到转阴的平均时间为8.56天(VS.对照组11.13天);4)安全性方面,VV116组无严重不良事件,安全性良好。 综上,从目前已完成的临床前研究、一期临床研究、真实世界研究和头对头三期临床研究来看,VV116具有良好的有效性和安全性,公司将积极推进VV116上市沟通进展及国际多中心临床试验的进度,争取持续为全球抗疫贡献中国力量。
问:A股再融资进展?
答:2022年4月,公司股东于2022年第一次临时股东大会通过议案,建议根据一般授权向特定对象发行不超过7,000万股股股票,所得款项预计不超过人民币39.69亿元,募集资金拟用于创新药研发项目及我们的科技总部及研发基地项目。
目前,公司2022年度向特定对象发行股股票相关事项正在正常推进中,尚需获得上海证券交易所审核通过及中国证券监督管理委员会同意注册。若后续获得证监会同意注册,公司将在有效期内,根据询价情况、市场情况及公司资金需求择机发行。
问:抗BTLA单抗进展及预期?
答:Tifcemalimab(TB004/JS004)是公司自主研发的全球首个进入临床开发阶段的抗肿瘤抗BTL单抗。截至目前,国内外尚无公开披露的其他同靶点抗肿瘤产品进入临床试验阶段。2022年6月,tifcemalimab在SCO年会上领衔亮相,首次展示了用于淋巴瘤与实体瘤治疗的早期临床成果,成为BTL靶点药物在肿瘤领域重要的里程碑事件。其中
(1)tifcemalimab单药治疗晚期实体瘤患者的Ia期剂量递增研究中,截止2022年4月30日,在19例可评估患者中,观察到1例部分缓解(PR)(黑色素瘤),7例疾病稳定(SD)(RECIST v1.1评估标准),且SD患者的中位持续时间为18周。该例PR的黑色素瘤患者,先前接受过纳武利尤单抗和BRF/MEK抑制剂治疗,在接受tifcemalimab后持续缓解已超过18个月,有长期有效趋势; (2)tifcemalimab单药或与特瑞普利单抗联合用于复发/难治性淋巴瘤的I期研究中,截止2022年4月26日,接受单药治疗的25名可评估患者中,观察到1例PR(滤泡性淋巴瘤),7例SD(2014版Lugano评效标准);接受联合治疗的6名可评估患者中(均为接受抗PD-1抗体治疗后进展患者),观察到3例PR(ORR 50%),1例SD。 上述数据可以初步体现tifcemalimab的临床疗效,其与特瑞普利单抗的联合,是一种极具前景的抗癌治疗策略,有望增加患者对免疫治疗的反应,扩大可能受益人群的范围。 目前,tifcemalimab已进入Ib/II期剂量扩展阶段,于中国和美国两地正在开展tifcemalimab和特瑞普利单抗在多个瘤种(复发/难治性淋巴瘤、黑色素瘤、头颈部鳞癌、鼻咽癌、肺癌等)当中的联合用药试验。若取得好的结果,公司将尽快开展和中美两地药监部门的沟通,争取于2023年将tifcemalimab推进到关键注册临床阶段。
问:抗TIGIT单抗与抗CD112R单抗的研发进度?后续联用策略?
答:CD112R是公司发现的全新免疫检查点通路,拥有该通路原始知识产权。CD112R与TIGIT的共同配体CD112表达于抗原递呈细胞和部分肿瘤细胞表面,CD112R与配体结合后可抑制T细胞和NK细胞的抗肿瘤作用。
公司的抗TIGIT单抗TB006(JS006)于2021年分别获得中美临床批准,但并未非常匆忙地推进,公司认为,充分发掘TIGIT通路,需要CD112R的相关研究参与,利用CD112R抑制剂与TIGIT、PD-1抑制剂联合治疗,可进一步促进T细胞活化,有望改善临床治疗效果。2022年4月与2022年8月,抗CD112R单抗TB009(JS009)的临床试验申请亦分别获得FD和NMP的批准,公司将加速推进抗TIGIT单抗、抗CD112R单抗单药及联合特瑞普利单抗的临床探索,以最大程度地发挥自主研发产品的协同抗肿瘤作用。
问:小核酸药物后续的适应症考量?
答:现阶段siRN药物仍以肝靶向为主要方向,公司早期适应症也以肝靶向、代谢类为主。针对混合型高脂血症开发的JS401为潜在国内首个该靶点siRN药物,可以长期有效针对混合型高脂血症。公司计划于近期提交该药物的Pre-IND。
目前公司的siRN药物研发平台已初步搭建完毕,后续公司计划利用抗体和其他技术,在现有平台基础上进一步探索靶向肝脏以外器官的可能性。
君实生物主营业务:创新药物的发现和开发,以及在全球范围内的临床研发及商业化
君实生物2022中报显示,公司主营收入9.46亿元,同比下降55.26%;归母净利润-91240.5万元,同比下降9861.53%;扣非净利润-94636.44万元,同比下降735.05%;其中2022年第二季度,公司单季度主营收入3.17亿元,同比下降36.61%;单季度归母净利润-51600.95万元,同比下降40.23%;单季度扣非净利润-51678.11万元,同比下降8.94%;负债率23.84%,投资收益85.07万元,财务费用-4279.18万元,毛利率67.59%。
该股最近90天内共有14家机构给出评级,买入评级13家,增持评级1家;过去90天内机构目标均价为98.18。
以下是详细的盈利预测信息:
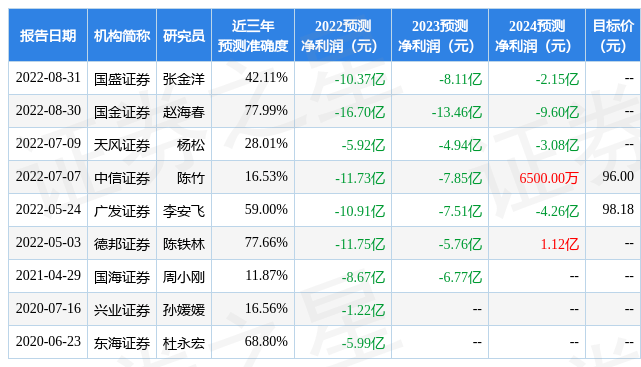
融资融券数据显示该股近3个月融资净流出2.23亿,融资余额减少;融券净流出2.43亿,融券余额减少。根据近五年财报数据,证券之星估值分析工具显示,君实生物(688180)行业内竞争力的护城河优秀,盈利能力较差,营收成长性较差。财务可能有隐忧,须重点关注的财务指标包括:应收账款/利润率、应收账款/利润率近3年增幅、经营现金流/利润率。该股好公司指标0.5星,好价格指标1星,综合指标0.5星。(指标仅供参考,指标范围:0 ~ 5星,最高5星)
以上内容由证券之星根据公开信息整理,与本站立场无关。证券之星力求但不保证该信息(包括但不限于文字、视频、音频、数据及图表)全部或者部分内容的的准确性、完整性、有效性、及时性等,如存在问题请联系我们。本文为数据整理,不对您构成任何投资建议,投资有风险,请谨慎决策。